| A.100g质量分数为46%的乙醇水溶液中,含有4NA个氧原子 |
| B.1mol Cl2溶于水,溶液中Cl-、HClO、ClO-粒子数之和小于2NA |
| C.2.24 L(标准状况)2H2中含有0.2NA个中子 |
| D.25℃时Ksp(CaSO4)=9×10-6,则该温度下CaSO4饱和溶液中含有3×10-3NA个Ca2+ |
| A.n(H2CO3)和n(HCO3-)之和为1mol的NaHCO3溶液中,含有Na+数目为NA |
| B.17gH2O2所含非极性键数目为0.5NA |
| C.标准状况下,H2和CO混合气体8.96L在足量O2中充分燃烧消耗O2分子数为0.2NA |
| D.56g 铁与足量氯气反应,氯气共得到3NA个电子 |
 ,且x+y+z=1.充电时电池总反应为LiNixCoyMnzO2+6C(石墨)= Li1-aNixCoyMnzO2+LiaC6,其电池工作原理如图所示,两极之间有一个允许特定的离子X通过的隔膜。下列说法正确的是
,且x+y+z=1.充电时电池总反应为LiNixCoyMnzO2+6C(石墨)= Li1-aNixCoyMnzO2+LiaC6,其电池工作原理如图所示,两极之间有一个允许特定的离子X通过的隔膜。下列说法正确的是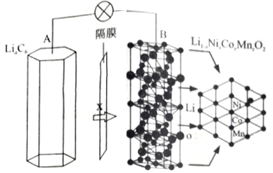
| A.允许离子X通过的隔膜属于阴离子交换膜 |
| B.充电时,A 为阴极,Li+被氧化 |
| C.可从无法充电的废旧电池的石墨电极中回收金属锂 |
| D.放电时,正极反应式为 Li1-aNixCoyMnzO2+aLi ++ae-= LiNixCoyMnzO2 |
| A.常温常压下, 30 g乙烷中所含的极性共价键数为6NA |
| B.0.1mol Fe与足量盐酸反应,转移的电子数为0.3NA |
C.0.1 mol Sr原子中含中子数为3.8NA Sr原子中含中子数为3.8NA |
| D.0.1mol·L-1的NH4NO3溶液中含有的氮原子数为0.2NA |
| A.化学的特征就是认识分子和制造分子 |
| B.波义耳提出化学元素的概念,标志着近代化学的诞生 |
| C.研究物质的性质常运用观察、实验、分类、比较等方法 |
| D.金属钠通常保存在煤油中,不能保存在石蜡油中 |
A.F-的结构示意图 | B.纯碱的化学式:NaHCO3 |
| C.过氧化钙的化学式:CaO2 | D.硫酸铁的电离方程式:Fe2(SO4)3=Fe23++3SO42- |
| A.K+、Na+、NO3-、MnO4- | B.Na十、Ca2+、NO3-、Cl- |
| C.K+、Na十、SO42-、NH4+ | D.K+、Na+、HCO3-、SO42- |
| 选项 | 古诗或谚语 | 含有的化学反应类型 |
| A | 熬胆矾之铁釜,久之亦化为铜 | 复分解反应 |
| B | 千锤万凿出深山,烈火焚烧若等闲 | 分解反应 |
| C | 春蚕到死丝方尽,蜡炬成灰泪始干 | 化合反应 |
| D | 爆竹声中除旧岁,春风送暖入屠苏 | 非氧化还原反应 |
| A.将盐卤或石膏加入豆浆中制成豆腐 |
| B.一枝钢笔使用两种不同型号的蓝黑墨水,易出现堵塞 |
| C.向FeCl3溶液中加入NaOH溶液,会出现红褐色沉淀 |
| D.静电除尘净化空气,提升空气质量 |
| A.三种分散系中分散质微粒都带电荷 |
| B.加热蒸干并灼烧,得到的产物都是三氧化二铁 |
| C.FeCl2、FeCl3溶液能稳定存在,而Fe(OH)3胶体不能稳定存在 |
| D.一定条件下可完成转化:FeCl2溶液→FeCl3溶液→Fe(OH)3胶体 |