| A.0.1 mol Fe在0.1 mol氯气中充分燃烧时转移的电子数为0.3NA |
| B.0.1 L 3.0 mol·L-1的NH4NO3溶液中含有的N原子数目为0.6NA |
| C.64 g的SO2与足量的O2充分反应后可得到NA个SO3分子 |
| D.标准状况下,2.24 L四氯化碳含有的分子数目为0.1NA |
| | 目的 | 操作 |
| A. | 取20.00 mL盐酸 | 在50 mL酸式滴定管中装入盐酸,调整初始读数为30.00 mL后,将剩余盐酸放入锥形瓶 |
| B. | 探究浓度对化学反应速率的影响 | 常温,向两只相同的试管中分别加入5mL0.1mol/L的KMnO4溶液,再分别加入2mL0.01mol/L的H2C2O4和2mL0.02mol/L的H2C2O4溶液,观察KMnO4溶液褪色所需要的时间。 |
| C. | 测定醋酸钠溶液pH | 用玻璃棒蘸取溶液,点在湿润的pH试纸上 |
| D. | 配制氯化铁溶液 | 将氯化铁固体溶解在较浓的盐酸中再加水稀释 |
   | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | | | | ① | ② | | ③ | |
| 3 | | ④ | ⑤ | | | ⑥ | ⑦ | ⑧ |
| 4 | ⑨ | | | | | | ⑩ | |
| 实验步骤 | 实验现象与结论 |
| ____________________ | ____________________ |
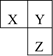
| A.Z 元素的氧化物对应的水化物一定是一种强酸 |
| B.在三种元素形成的气态氢化物中,Y 的气态氢化物最稳定 |
| C.三种元素原子半径的大小顺序为:X>Y>Z |
| D.Z 的单质与 Fe 反应生成的化合物中,铁元素显+3 价 |
| A.在金属元素与非金属元素的分界线附近可以寻找制备超导体材料的元素 |
| B.在过渡元素中可以寻找制备催化剂及耐高温、耐腐蚀材料的元素 |
| C.在过渡元素区域可以寻找制备新型农药材料的元素 |
| D.非金属性最强的元素在元素周期表的最右上角 |
A.C+CO2 2CO 2CO | B.2Al+Fe2O3 2Fe+Al2O3 2Fe+Al2O3 |
C.C+H2O CO+H2 CO+H2 | D.CaCO3 CaO+CO2↑ CaO+CO2↑ |
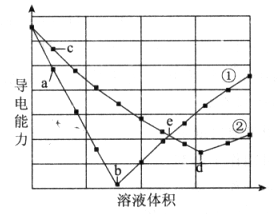
| A.①代表滴加Ba(OH)2溶液的变化曲线 | B.a、c两点,溶液中均大量存在H+和SO42- |
| C.b、d两点对应的溶液均显中性 | D.e点,两溶液中含有相同量的OH- |
| A.将剩余的金属钠丢弃在废纸篓里 |
| B.少量酒精洒在桌子上着火时,立即用湿布扑灭 |
| C.闻气体时,用手轻轻扇动使少量气体飘进鼻孔 |
| D.稀释浓硫酸时,将浓硫酸沿器壁缓慢注入水中并不断搅拌 |
| A | B | C | D |
| 汽油 | 天然气 | 浓硫酸 | 氢氧化钠 |
 |  |  |  |
| 实验 | 现象 | 结论 |
| A.用铂丝蘸取某金属的盐溶液,在酒精灯火焰上灼烧 | 火焰呈黄色 | 此盐溶液中含有 Na+,不含 K+ |
| B.①取少量绿矾样品,加水溶解,滴加 KSCN 溶液 ②向溶液中通入空气 | ①溶液颜色无变化 ②溶液逐渐变红 | ①绿矾样品未变质 ②Fe2+易被空气氧化为 Fe3+ |
| C.①某溶液中加入 Ba(NO3)2溶液 ②再加入足量盐酸 | ①产生白色沉淀 ②仍有白色沉淀 | 原溶液中有 SO42﹣ |
| D.向碘水中加入等体积 CCl4, 振荡后静置 | 上层接近无色,下层显紫红色 | I2 在 CCl4中的溶解度小于在水中的溶解度 |